Is éard is intuaslagthacht ann maoin de shubstaint a thuaslagadh in uisce nó i dtuaslagóir eile. Is féidir le substaintí soladacha agus leachtacha agus gásacha a thuaslagadh in uisce. De réir intuaslagthachta, roinntear na substaintí go léir i dtrí ghrúpa:
- an-intuaslagtha
- beagán intuaslagtha
- dothuaslagtha
Níl substaintí atá dothuaslagtha go hiomlán ann, dá bhrí sin tá an t-ainm dothuaslagtha coinníollach agus ní mór duit "dothuaslagtha go praiticiúil" a léamh.
Braitheann intuaslagthacht substaintí ar theocht ar theocht agus ar bhrú, mar shampla, an tsubstaint KNO3 (níotráit photaisiam) ag teocht + 20 ° C tá intuaslagthacht 31.6 g / 100 g uisce ann, agus ag teocht + 100 ° C - 245 g / 100 g uisce.
Intuaslagthacht, deascadh agus hidrealú salainn faoi ghnáthchoinníollacha

Mínithe ar an tábla:
- P - tá salann intuaslagtha (níos mó ná 0.1 mol / l),
- M - salann intuaslagtha go géar (0.1-0.001 mol / l),
- N - salann dothuaslagtha (níos lú ná 0.001 mol / l),
- [N] - hidrealú dochúlaithe, ní thagann an salann as an tuaslagán, deascann an príomh-salann le scaoileadh dé-ocsaíd charbóin, Cr2S.3 - deascán Cr (OH)3 le scaoileadh sulfíde hidrigine,
- + - imoibríonn salann go hiomlán le huisce,
- - - Gan a bheith ann,
- * P - a hidrealú le cation,
- P * - hidrealaithe ag an anion.
Intuaslagthacht salainn
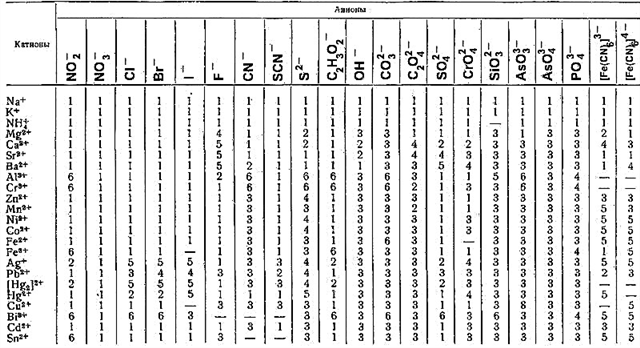
Mínithe ar an tábla
- 1 - tá salann intuaslagtha in uisce,
- 2 - beagán intuaslagtha in uisce,
- 3 - dothuaslagtha in uisce, ach intuaslagtha in aigéid orgánacha agus mianracha,
- 4 - dothuaslagtha in uisce agus in aigéid orgánacha, ach intuaslagtha in aigéid mhianracha,
- 5 - níl an salann dothuaslagtha in uisce ná in aigéid,
- 6 - hidrealú.
Más maith leat an suíomh, beimid buíoch as an tóir a bhí air :) Inis do do chairde fúinn ar an bhfóram, ar bhlag, ar phobal. Seo an cnaipe atá againn:
Cód Cnaipe: